電解水是一種通過電解液態水或水蒸氣來產生氫氣和氧氣的技術。在1 bar的壓力下,液態電解槽的工作溫度通常介于0℃(冰的熔點)和100℃(水的沸點)之間。然而,由于反應動力學的限制,實際運行中通常不會將電解槽冷卻至低于標準溫度(25℃)。為了降低電解槽的內阻,液態水的電解溫度一般控制在50℃至90℃之間,同時還需考慮電解槽材料的穩定性。通過使用自增壓電解槽,液態水的溫度甚至可以超過100℃,但超過某一臨界點后,只能電解水蒸氣。這種工作條件被稱為“近環境溫度與壓力”(Near Ambient Temperature and Pressure, NATP)條件。
電解液態水時,通常使用pH值在0(強酸性)到14(強堿性)之間的電解質。由于中性電解質缺乏足夠的載流子(Charge Carriers, CC),其在實際應用中并不受青睞。為了提高電解效率,通常選擇遷移率較高的離子作為載流子,如質子(H?)或羥基離子(OH?)。質子具有更高的遷移率,這得益于其特有的跳躍傳輸機制(Grotthuss機制)。雖然羥基離子的遷移率僅為質子的1/16,但通過使用高濃度的氫氧化鉀(KOH)水溶液,可以有效提高其離子遷移率,從而提升電解效率。
在不同pH條件下,水分解的半反應式如下:
在酸性條件下:
- 陽極反應:H?O → ?O? + 2H? + 2e?
- 陰極反應:2H? + 2e? → H?
在堿性條件下:
- 陽極反應:2OH? → ?O?+ H?O + 2e?
- 陰極反應:2H?O + 2e?→ H?+ 2OH?
半反應的電極電勢會隨著電解液pH值的變化而變化。如下圖所示,在堿性介質中,電極電勢沿電勢軸向下移動,進入pH電位鈍化區,此時過渡金屬(如鎳、鐵)表面形成鈍化膜,從而獲得保護。因此,廉價的過渡金屬可以作為催化劑、管路和電解槽組件使用。而在酸性電解液中,電極電勢向上移動,進入反鈍化區,過渡金屬失去保護,容易被腐蝕。因此,在酸性條件下,需要使用耐酸的貴金屬(如鉑族金屬)作為電催化劑。
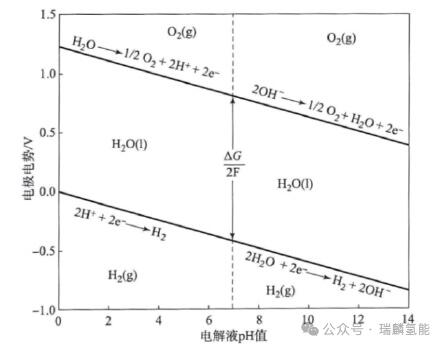
圖:半室反應電極電勢隨電解液 PH值變化而變化的曲線
為避免腐蝕問題并降低設備成本,近年來更傾向于采用類似固體聚合物電解質(SPE)概念的“駐留電解質”系統,而非循環酸性電解液。這種設計可以減少對昂貴材料的依賴,并降低對電解槽部件、管路及輔助設備(Balance of Plant, BoP)的腐蝕風險。
綜上所述,電解液的pH值不僅影響電解反應的速率和效率,還決定了所需材料的種類與成本。因此,在實際應用中,需要綜合考慮電解效率、材料成本、設備壽命等因素,選擇最合適的電解質體系。